|
3 電泳檢定法︰ |
|||
|
3.1 電泳原理: |
TOP ▲ |
||
|
蛋白質的泳動率 |
|||
|
a. 泳動率 |
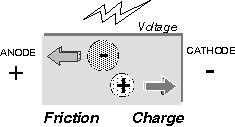
帶電分子在電場中會被電流移動,是為 泳動;其泳動的大小程度稱為 泳動率 (mobility)。泳動率與分子上 電荷密度 成正比,而與其分子 摩擦力 成反比: (所外加 電壓 mV) × (分子之 淨電荷密度) 泳動率 ∼ ───────────────── 分子與介質間之 摩擦力 上述之摩擦力,決定於此分子之 大小、形狀。 分子量大者摩擦力大,泳動率小;球形分子摩擦力較小,泳動率大。 |
||
|
b. 蛋白質的帶電性 |
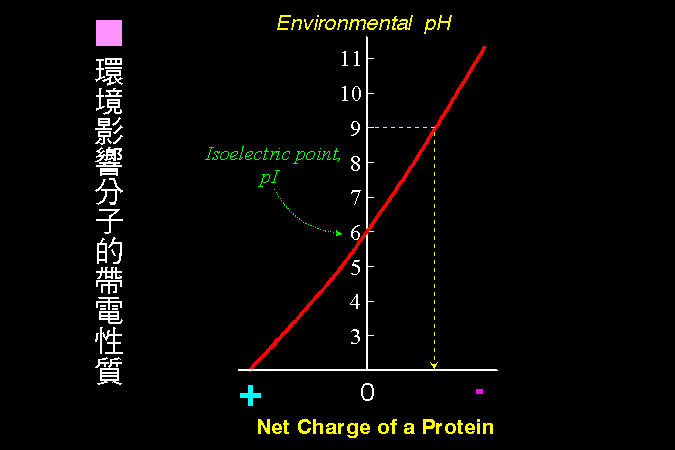
蛋白質分子上的淨電荷,取決於 環境 pH 高低;若環境 pH 高於其 pI,此蛋白質帶淨負電,反之帶淨正電;若剛好等於其 pI,淨電荷為零 (正電數目等於負電)。同一分子在不同 pH 環境下,可能帶不同 淨電荷 (圖 3.1)。 |
||
|
圖 3.1 環境 pH 的影響 |
|||
|
c. 蛋白質由負極向正極泳動 |
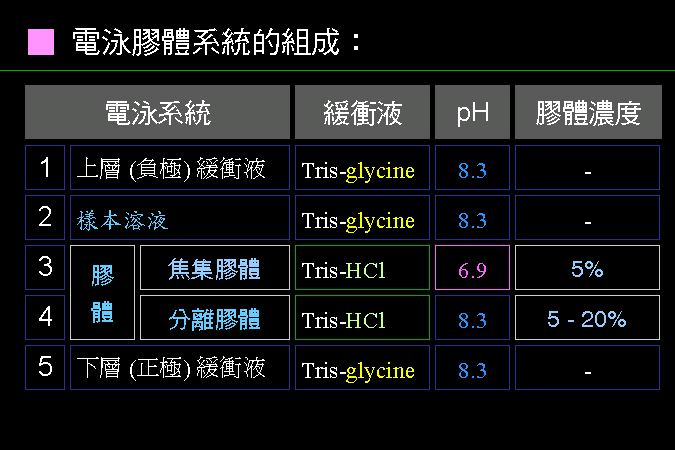
電泳系統中,電子由負極流向正極; 帶負電的分子往正極跑,帶正電的分子往負極跑,不帶電者則不易泳動。大部分電泳系統的 pH 定在 8.3,在此 pH 下,凡是 pI 小於 8.3 的分子均帶負電荷,可以往正極跑。 |
||
|
d. 外在條件影響泳動率的因素 |
促進泳動: |
低膠体濃度 (孔徑大)、低濃度緩衝液、高電壓、高電流、高溫。 |
|
|
降低泳動: |
上述各點的相反條件、樣本含高濃度鹽類、樣本 pH 太高或太低。 |
||
|
TOP ▲ |
|||