酵素講義總目錄
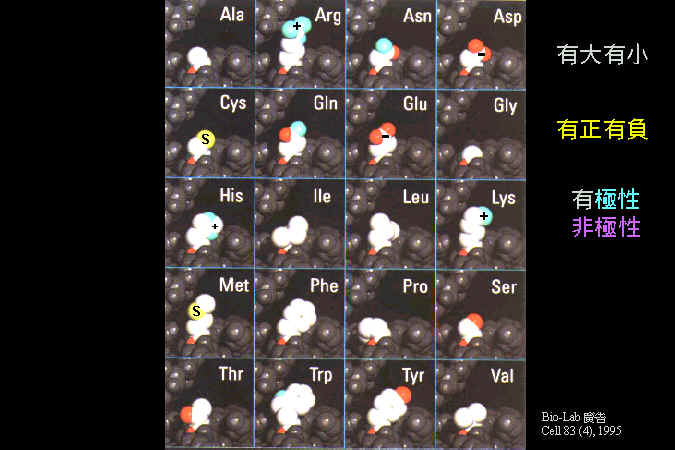
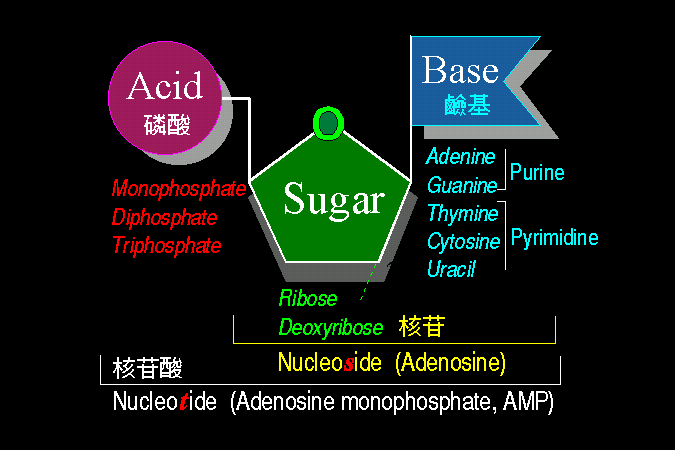
清楚瞭解蛋白質的構造,對學習酵素而言非常重要;我假設同學對蛋白質的構造與性質,都有很好的基礎背景。因此除非必要,將不會再講到蛋白質的四級結構與其性質,請自行 複習 上一部份的教材。
我們上課的進度將以所發的講義為主,其中各章節的編排方式,與所用的課本不太一樣,但應可找出互相對應的部份,請勿忽略閱讀課本文字。酵素部份的上課內容,也將全程以幻燈片講解;幻燈片的內容來自十多本教科書,希望能找到最好、最容易瞭解的圖片,來說明生物化學中有關酵素的種種有趣現象。雖然講義中寫有酵素在生物技術上的一些應用例 (第八節) ,但因時間關係在課堂上無法講述,僅供同學參考之用。
為了方便同學們找到這些資料,我把圖片 集中 影印,並且加上自行編製的圖表及說明,收集成冊以利同學課餘研讀。雖然如此,課堂上的講習仍然是最重要的,因為可以很快速給同學們整體且鮮明的觀念。
用幻燈片上課甚為直接而有效,但因燈光昏暗以致同學容易入睡;請在上課前一天早早入睡,次日一早提前到課堂預習上課,則必能大有收穫。亦不妨以咖啡或濃茶提神,甚或懸樑刺股,均可一試。
■ 到講義相關部份