|
胺基酸基本構造: |
|
|
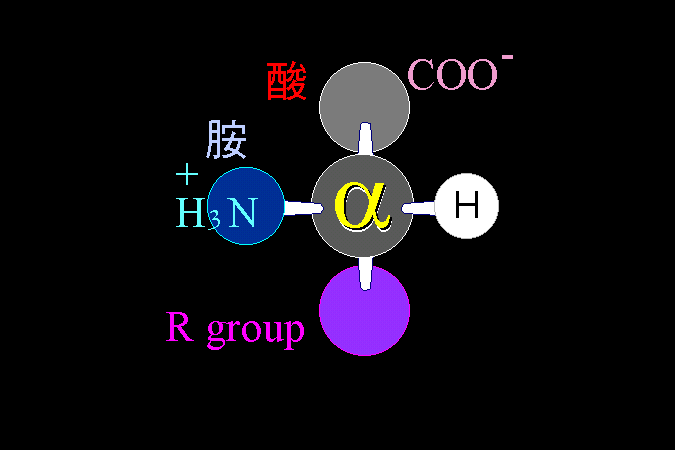
胺基酸種類很多,但有共同的基本構造;先畫一個十字,如下述方法在四端加上四個化學基團即可。 圖 1 為其基本構造,注意單醣也有類似的基本架構。 |
|
|
|
圖 1 胺基酸的基本構造 |
|
當你忘記胺基酸的構造時,畫個十字奇蹟馬上出現。你只要在這十字的中央填上一個碳原子 (叫做 a 碳),在周圍的四個位置分別填上一個氫原子、胺基、羧基及一個 R 基團,基本的胺基酸構造即完成。 |
|
|
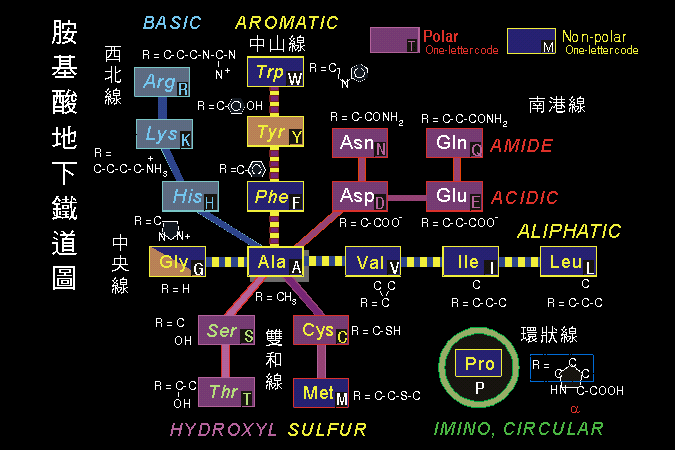
R 基團可以由最簡單的 H 開始填入,就是最簡單的 glycine;再來是 CH3 就是 alanine;如此越來越大,並加入其它種類的原子 (如氧或硫),或額外的胺基或羧基,就可以組成多采多姿的二十種胺基酸。 |
|
|
請注意 a 碳是不對稱的,因為它周圍的四個原子或基團都不相同;只有當 R 基團為氫原子時,是對稱的 a 碳 (因為接有兩個一樣的氫原子);也就是說只有 glycine 是對稱的胺基酸。 因此,除了 glycine 外,其它胺基酸都有其立體異構物,兩立體異構物間的化學式完全一樣,但互相成為鏡像,胺基酸的立體異構物以 L- 及 D-form 來表示之;地球上的生物大都採用 L-from 胺基酸。 |
|
|
a. |
分子構造的中心為一碳原子,稱為 a 碳 (a carbon)。 |
|
b. |
接在 a 碳上,有一個 胺基 及一個 酸基 (故名胺基酸)。 |
|
c. |
另有一氫原子及一基團 (R) 接在 a 碳上 (碳為 sp3 軌道)。 |
|
d. |
a 碳接了四個不同的基團,為 不對稱碳,有 光學異構物 (D/L)。 通常細胞的代謝只使用 L 型胺基酸,但有些細菌細胞壁或抗生素上,有 D 型胺基酸。 |
|
e. |
隨 R 基團的不同,各胺基酸的性質互有差異,組成二十種胺基酸 (見表 1)。 |
|
◆ 碳原子的 sp3 軌道,是整個蛋白質構造化學的根本,請探討其組成及立體構型。 |
|
|
◆ 辨別一個胺基酸時,請先抓出 a 碳,再以此為中心辨認胺基、酸基及 R 基團。當胺基酸組成蛋白質後,胺基與酸基都用來鍵結,連有 R 基團者即為 a 碳。 |