|
生物化學基礎 Biochemistry Basics 2008 胺基酸 Amino Acid |
回首頁 ■ |
||
|
|
|||
|
目 錄 |
1 胺基酸基本構造 2 胺基酸分類 表 1 二十種胺基酸的分類及性質 3 胜肽 4 胺基酸離子性質 4.1 解離常數 (pKa) 4.2 等電點 (pI) |
神奇的 peptide bond 平面可能是生命與無生物的臨界點 |
Amino acid (中文) |
|
■ 胺基酸 |
■ 相關投影片 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
胺基酸是構成蛋白質的基本單位,而蛋白質是生物体內最重要的活性分子,其中擔任催化種種生理代謝反應的酵素,更是近代生物化學的研究重心。二十種性質各異的胺基酸,連接成多樣的蛋白質,且賦予蛋白質特定分子構形,使蛋白質分子能夠具有生化活性。
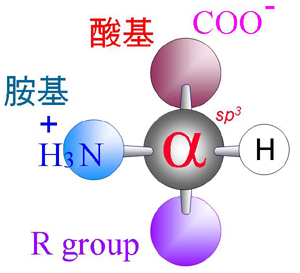
圖 1 胺基酸的基本構造 |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
1 胺基酸基本構造:胺基酸種類很多,但有共同的基本構造;先畫一個十字,如下述方法在四端加上四個化學基團即可。圖 1 為其基本構造,注意單醣也有類似的基本架構。 a. 分子構造的中心為一碳原子,稱為 a 碳 (a carbon)。 b. 接在 a 碳上,有一個胺基及一個酸基 (故名胺基酸)。 c. 另有一氫原子及一基團 (R) 接在 a 碳上 (碳為 sp3 軌道)。 d. a 碳接了四個不同的基團,為不對稱碳,有光學異構物 (D/L)。通常細胞內代謝只使用 L 型胺基酸,但有些細菌細胞壁或抗生素上,有 D 型胺基酸。 e. 隨 R 基團的不同,各胺基酸的性質互有差異,組成 20 種常用胺基酸 (下表 1)。 ◆ 碳原子的 sp3 軌道,是整個蛋白質構造化學的根本,請探討其組成及立體構型。 ◆ 辨別一個胺基酸時,請先抓出 a 碳,再以此為中心辨認胺基、酸基及 R 基團。當胺基酸組成蛋白質後,胺基與酸基都用來鍵結,連有 R 基團者即為 a 碳。
|
[投影片 A1]
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
2 胺基酸分類:胺基酸由其 R 基團的化學構造不同,可分為數大類。 a. 胺基酸的基團形形色色,有大有小、有直鏈有環狀、有正有負也有不帶電。表 1 列出蛋白質所用的 20 種胺基酸,是以 R 基團的化學構造來分組。 b. R 基團也可以其極性大小來分類,代表它們親水性的強弱;可把胺基酸分為極性及非極性兩大類,極性者又分為酸性、中性、鹼性三類。 c. 胺基酸本身的性質,以及所組成蛋白質分子的功能與性質,均決定於 R 基團的本質;這點在說明蛋白質的構造時,更是重要。 ◆ 把 20 種胺基酸的構造多寫幾次,注意 R 基團的極性、大小與其特殊官能基。
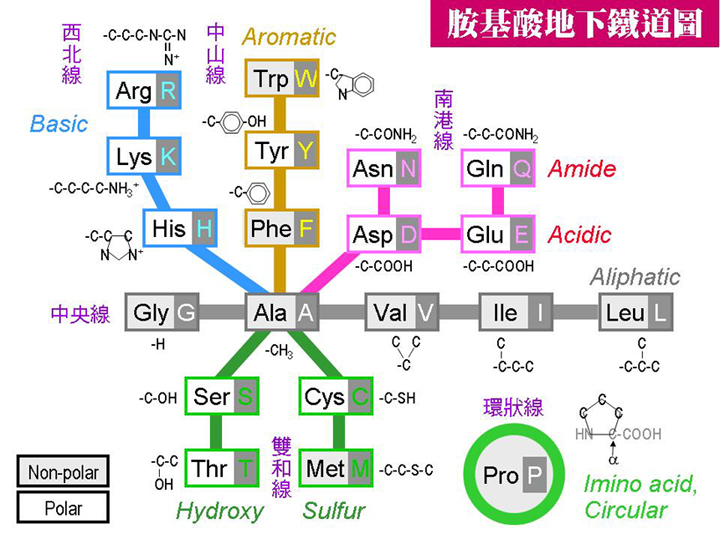
(1) 打有 * 者是人類的必需胺基酸,須由外界攝取。N, non-polar 非極性; P, polar 極性。 (2) 兩分子胱胺酸 (Cys) 以雙硫鍵連成二元体 (雙胱胺酸)。 (3) 這兩個胺基酸對蛋白質的立體構造有很大的影響。
圖 2 各種胺基酸的分類 圖 2 是特地設計用來說明各胺基酸的構造關係,不是代謝途徑,請特別注意。 圖中把各種胺基酸依其 R 基團的性質不同分類,並安排在台北市地下鐵的模擬地圖上,其中 Ala 是台北總站,因為其他的胺基酸都可由此分畫出來。中央線即為忠孝東路線,由飽和碳氫鏈的胺基酸所組成,與忠孝東路的商業機能有類比關係。 |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
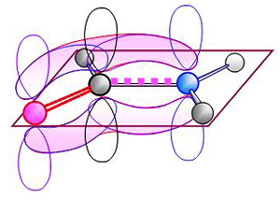
3 胜肽:胜肽是較短的蛋白質,許多胜肽有重要的生物功能或活性。 a. 胜肽鍵 (peptide bond) 是由一個胺基酸的酸基,與次一胺基酸的胺基,行脫水縮合反應而成的 C-N 鍵,具有雙鍵的性質,與相鄰總共六個原子在同一平面上,因此 C-N 鍵不能自由轉動。胜肽鍵是構成蛋白質架構的基本單位,非常重要,請注意研究其立體構成。 ◆ 練習畫出胜肽鍵的化學構造,注意胜肽鍵平面上各原子的相對位置,不要弄錯。 b. 兩個胺基酸以胜肽鍵連成的二元体,稱之為雙胜 (dipeptide),三個胺基酸則以兩個胜肽鍵連成三胜 (tripeptide),許多胺基酸連成多胜 (polypeptide);再大的胜肽即為蛋白質。 ◆ 含有多少個胺基酸才能叫做蛋白質?並沒有公定的數目,通常幾十個胺基酸長度者可稱為胜肽,而百個以上即稱蛋白質,在這中間的就自行決定。 c. 某些胺基酸或胜肽具有較特殊的生理活性,如味素 (Glu)、腦啡以及部份荷爾蒙等。
◆ 大腦神經如何受到化學物質的控制 (一小段影片取自 Discovery 大腦與感官) wmv, 10 min, 14 Mb
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
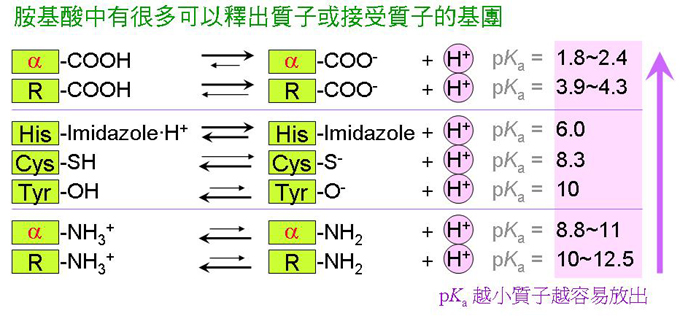
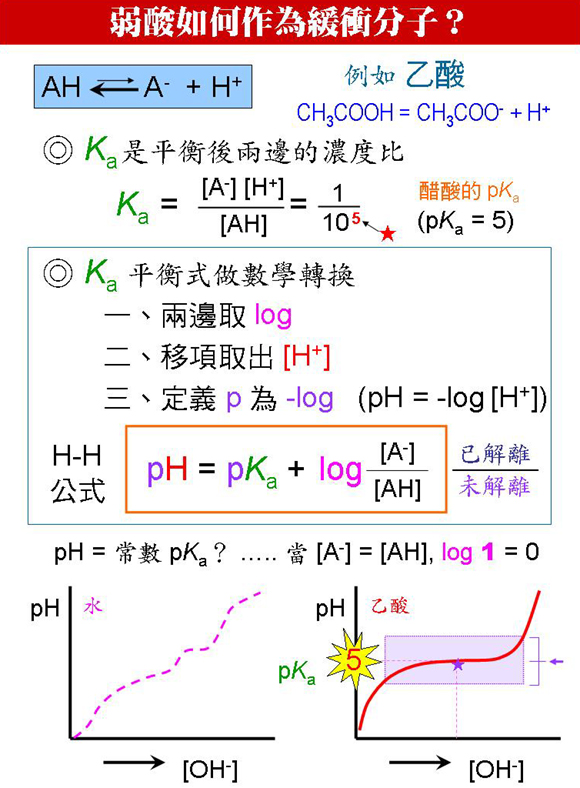
4 胺基酸的離子性質:胺基酸多以離子狀態存在,且經常同時帶有正電及負電基團。 4.1 解離常數 (pKa): 質子是化學層次最小的粒子,很容易由一極性基團解離出來,在水溶液中無所不在;其解離難易可以解離常數 (pKa) 表示,越小越容易解離,水的 pKa 在 6~7 之間。 a. 質子搶奪:氫原子若與陰電性大的原子 (如酸基 -COOH 中的氧原子) 共價,則其電子易遭搶奪而使質子裸露 (-COO- H+),進而解離出 H+。質子易受帶有高電子密度的基團 (如 -NH2) 所吸引,使後者成為一帶正電基團 (-NH3+)。 b. Ampholyte:胺基酸的酸基易解離出質子 (成為帶負電基團 -COO-),而其胺基又會接受一質子 (成為 -NH3+)。如此一分子同時帶有正電與負電者,稱為 ampholyte (兩性離子)。 c. 質子解離:質子解離程度決定於該水溶液的 pH,與其分子上解離基團 pKa 的高低。 pKa 的大小,顯示一個官能基容不容易放出 H+,越小的越容易放出。圖 3 列出各種胺基酸的解離基團及其 pKa,請注意各種基團在不同的 pH 下解離。當環境的 pH 等於某基團的 pKa 時,該基團恰有一半數目的分子解離 (pH = pKa + log ([A-]/[HA]),請見 圖 4 說明。 圖 3 各種胺基酸基團的解離及其 pKa 4.2 等電點 (pI): 等電點是所有分子帶電性質的重要指標。 a. 胺基酸 a 碳上的胺基及酸基各有一帶電基團,故有二 pKa,分別界定胺基及酸基的解離 pH。此二 pKa 平均值即為該胺基酸的 pI (等電點),即 (pKa1 + pKa2) ÷ 2 = pI。 b. 若環境的 pH 等於某胺基酸的 pI,則此胺基酸的淨電荷為零;因為在此 pH 下,剛好有一正電基團及一負電基團。Ampholytes 若剛好淨電荷為零,則其正、負電基團數目相等,特稱為 Zwitterion。 c. 胺基酸的淨電荷是正或負,受環境的 pH 所控制;環境 pH > pI 帶負電,反之則帶正電。上一章圖 3 即說明此一影響,同時請注意,若環境的 pH 離該分子的 pI 越遠,則其所帶之正或負淨電荷越大。 d. 某些胺基酸的 R 基團,有額外的帶電基團 (例如 Lys 另有一胺基),則可有三個 pKa;即每個可解離出 H+ 或吸收 H+ 的官能基,都有一個 pKa。這三個 pKa 中,有兩個 pKa 的胺基酸各帶一個淨正電或淨負電,則這兩個 pKa 值的平均即為其 pI。 ◆ 練習畫出額外帶有電荷胺基酸的 pKa 滴定曲線,並觀察其電荷改變情形。 e. 多胜在某 pH 下的淨電荷,是所組成胺基酸所帶電荷總和。例如一條十胜所含的 10 個胺基酸 (AELKVGRRDV) 中,若有 5 個胺基酸為非極性,3 個帶正電基團,兩個帶負電,則此十胜在中性 pH 下的淨電荷為 1 個正電。 圖 4 以乙酸為例說明緩衝分子如何在其 pKa 發揮作用 醋酸根會吸收或放出一個質子,可以用解離常數 Ka 描述之;對 Ka 進行數學轉換可得 Henderson-Hasselbalch 公式,此式描述當 [A-] 等於 [AH] 時,環境的 pH 恰等於乙酸的 pKa (= 5),有最大的緩衝效果。 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
問題集 以下題目不一定有標準答案,甚至會引起很大的爭議,但這就是問題集之目的。1. 請畫出一個胜肽鍵 peptide bond 的構造,並以點線標出 peptide平面。 2. 為何胜肽鍵平面不能自由轉動? 3. Histidine 有三個可以解離的基團,其 pKa 分別是 1.8, 6.0 及 9.2,請問其 pI 多少? 4. 同上題,Histidine 能否用來作為中性 pH 的緩衝液之用?並請說明為何。 5. 請依括號內的指示寫出下列各胺基酸有何特點或用途: Glutamate (食品) Serine (轉譯後修飾) Tryptophan (藥品) Cysteine (蛋白質三級構造) Proline (蛋白質二級構造) 6. 以下兩段胜肽有何異同之處?並請問二者的滴定曲線會不會一樣?為什麼? Ser-Glu-Gly-His-Ala; Gly-His-Ala-Glu-Ser 7. 請判斷並說明下列各題的真偽: a. 胺基酸的 a 碳都是不對稱碳。 b. 下列胺基酸的 R 基團為非極性者:Ala, Val, Ile, Leu。 c. 下列胺基酸的 R 基團都帶有正電荷:Asp, Lys。 d. 下列胺基酸的 R 基團帶有硫原子或氧原子:Cys, Ser, Thr, Met。 e. 兩個胺基酸可以氫鍵連成雙胜。 f. 蛋白質分子是活動的,因兩為個胜肽平面之間是單鍵。 g. 胺基酸分子所帶的電荷不會改變。 h. 胺基酸可作為緩衝液是因為其基團官能基是一種強酸。 i. 胺基酸在其等電點時沒有帶任何電荷在分子上。 j. His 上 imidazole pKa 為 6.0,因此可作為細胞內的緩衝物質。 8. 寫出含有硫原子的胺基酸:(英文全名) 1______________ 2_______________ 寫出含有芳香基團的胺基酸: 1_______________ 2_______________ 3______________ 寫出含有醇基的胺基酸: 1_______________ 2_______________ 3______________ 寫出含飽和碳氫鏈的胺基酸: 1_______________ 2_______________ 3______________ 寫出側鏈基團帶有 -COOH 的兩種胺基酸: 1_______________ 2_______________ 9. 細胞的各種分子構造中,那些構造或分子含有氫鍵? 例如: a helix, 請再回答三個。 那些構造或分子含有疏水鍵? 例如:細胞膜 (請再回答兩個)。 10.有一段 peptide 序列如下: Glu-Phe-Lys-His-Ile-Arg-Val 在 pH = 1 時其淨電荷為 ____;在 pH = 7 時淨電荷為 _____; pH = 11 時淨電荷為 _____ 11.請不要看書或講義,畫出上題胜肽的分子構造。(請先畫出胜肽骨架,再填上 R 基團) 12.是非選擇題 (答案寫在□內,是→○、非→╳) 1) 在中性 pH 溶液中,那些胺基酸可做為此 pH 的緩衝分子? □ Val □ His □ Glu □ Trp 2) 在 pH 2 溶液中,那些胺基酸可做為此 pH 的緩衝分子? □ Val □ His □ Glu □ Trp 3) 下列何者為兩性 (amphoteric) 化合物? □ 胺基酸 □ 水分子 □ 蛋白質 □ DNA □ 葡萄糖 4) 有關 pKa 的性質描述: □ 解離常數 pKa 是一平衡常數 □ pKa 越高則質子越容易解離 □ pKa = 2 的基團在中性溶液下將會帶負電荷 □ 分子所帶的電荷固定不變 5) 下述碳原子何者為不對稱碳? □ CH4 □ glutamic acid 的 a 碳 □ 甘胺酸的 COOH □ 甘胺酸的 a 碳 6) 有關胜肽鍵的性質描述: □ 其前後八個原子成一平面 □ 胜肽鍵有 p 電子共振 □ 胜肽鍵可以自由轉動 □ 胜肽鍵是經加水反應生成的 13.寫出三個具生理功能的胜肽: 1_______________ 2_______________ 3______________ 14.當一個分子上的正電荷數目等於負電荷,此種離子狀態稱之為 _____________;而此時的 pH 則為此分子之 _______。 15.若某一弱酸的解離常數 pKa 為 5,若此弱酸被用來作為緩衝液分子,其適用範圍多少? 16.胺基酸單位是以代謝路徑被合成出來的,而蛋白質是以 DNA 為信息經由 RNA,把胺基酸連接起來轉譯而得;那麼大約含有十個胺基酸的胜肽是如何合成出來的?
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
■■■